فهرست مطالب
دانشمندان سرنخهای آلزایمر را در DNA پنهان یافتند که زمانی به عنوان “آشغال” نادیده گرفته میشدند
مقدمه:
به گزارش سرویس علمی فارماوب بیماری آلزایمر و ژن ها : بیشتر DNA ما ژنها را کد نمیکند، بلکه به عنوان سوئیچهایی عمل میکند که نحوه استفاده از ژنها را کنترل میکنند. محققان اکنون صدها مورد از این سوئیچها را در آستروسیت ها نقشهبرداری کردهاند و بسیاری از آنها را که ژنهای مرتبط با بیماری آلزایمر را تنظیم میکنند، یافتهاند.
توضیح مفید:
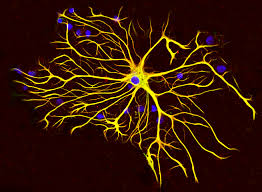
آستروسیت (astrocyte) یا آستروگلیا یا اختریاخته، یاختهای گلیایی و ستارهشکل است که تغذیه و حفاظت یاختههای عصبی را بر عهده دارد.
آستروسیتها سلولهای گلیای ستارهشکل در مغز و طناب نخاعی میباشند. آستروسیتها بیشترین نوع سلولهای گلیا هستند. آستروسیت یعنی سلول ستارهای و این نام به درستی شکل این سلول را توصیف میکند. آستروسیتها از اندازه بزرگی برخوردارند و نورونها را تغذیه کرده و از انها حمایت میکنند و به همراه میکروگلیاها مواد زاید درون مغز را از بین میبرند؛ و در نهایت به صورت مواد شیمیایی از مایع احاطهکنندهٔ نورونها حفاظت میکنند.
متن:
محققان سوئیچهای DNA گریزان را در سلولهای پشتیبان مغز شناسایی کردهاند که بر ژنهای مرتبط با بیماری آلزایمر تأثیر میگذارند.
وقتی مردم در مورد DNA فکر میکنند، اغلب ژنهایی را تصور میکنند که صفات فیزیکی ما را تعیین میکنند، بر رفتار تأثیر میگذارند و بدن ما را به درستی عملکرد میکنند.
در واقعیت، ژنها تنها بخش کوچکی از ماده ژنتیکی ما را تشکیل میدهند. تقریباً ۲٪ از DNA حاوی تقریباً ۲۰۰۰۰ ژنی است که انسان حمل میکند. ۹۸٪ دیگر که معمولاً به عنوان ژنوم غیر کدکننده یا DNA “زباله” شناخته میشود، عناصر تنظیمی زیادی را در خود جای داده است که تصمیم میگیرند چه زمانی ژنها روشن شوند و چقدر فعال شوند.
دانشمندان دانشگاه UNSW سیدنی اکنون توالیهای مهم DNA تنظیمی را که بر عملکرد آستروسیتها تأثیر میگذارند، مشخص کردهاند. آستروسیتها سلولهای پشتیبان در مغز هستند که به نورونها کمک میکنند و در بیماری آلزایمر نقش دارند.
در مطالعهای که در مجله Nature Neuroscience منتشر شد، محققان دانشکده بیوتکنولوژی و علوم بیومولکولی دانشگاه UNSW از آزمایش نزدیک به ۱۰۰۰ ناحیه تنظیمی کاندید به نام تقویتکنندهها در آستروسیتهای انسانی رشد یافته در آزمایشگاه خبر دادند. تقویتکنندهها قطعات کوتاهی از DNA هستند که میتوانند ژنها را از فواصل دور، گاهی صدها هزار حرف DNA دورتر، کنترل کنند، که از نظر تاریخی بررسی آنها را چالشبرانگیز کرده است.
وب گردی:
تومورهای مغزی: انواع، علائم و علل اصلی
تکنیک ها در مطالعه ی بیماری آلزایمر و ژن ها
برای انجام این کار، تیم CRISPRi، (CRISPRi روشی جدید برای مهار ژنهای خاص است. سیستم CRISPRi از یک نوکلئاز غیرفعال Cas9 (dCas9) متصل به ساختار سرکوبگر اختصاصی SALL1-SDS3 ما برای مسدود کردن رونویسی ژنهای هدف، بدون برش DNA، استفاده میکند) تکنیکی که میتواند مناطق خاص DNA را بدون برش آنها به طور موقت خاموش کند، را با توالییابی RNA تک سلولی که فعالیت ژن را در سلولهای منفرد ردیابی میکند، ترکیب کرد. با استفاده از این استراتژی، محققان توانستند عملکرد تقریباً ۱۰۰۰ تقویتکننده را به طور همزمان ارزیابی کنند.
دکتر نیکول گرین، نویسنده اصلی میگوید: “ما از CRISPRi برای خاموش کردن تقویتکنندههای بالقوه در آستروسیتها استفاده کردیم تا ببینیم آیا بیان ژن را تغییر میدهد یا خیر.”
«و اگر این اتفاق میافتاد، میدانستیم که یک تقویتکننده عملکردی پیدا کردهایم و سپس میتوانستیم بفهمیم کدام ژن – یا ژنها – را کنترل میکند. این اتفاقی بود که برای حدود ۱۵۰ مورد از تقویتکنندههای بالقوهای که آزمایش کردیم، افتاد. و نکته جالب توجه این است که بخش بزرگی از این تقویتکنندههای عملکردی، ژنهای دخیل در بیماری آلزایمر را کنترل میکردند.»
با افزایش ۱۰۰۰ کاندید به ۱۵۰ سوئیچ واقعی، دانشمندان به طور چشمگیری محدود میشوند که در ژنوم غیرکدکننده به دنبال سرنخهایی از ژنتیک بیماری آلزایمر باشند.
این یافتهها نشان میدهد که برای برجسته کردن تقویتکنندههای عملکردی در فضای وسیع DNA غیرکدکننده، به مطالعات مشابهی در سایر انواع سلولهای مغزی نیاز است.»
مطالعه بین خطوط
پروفسور ایرینا ووینگو، که بر این مطالعه نظارت داشت، میگوید که این نتایج، فهرستی از مناطق DNA را در اختیار محققان قرار میدهد که میتواند به تفسیر نتایج سایر مطالعات ژنتیکی نیز کمک کند.
او میگوید: «وقتی محققان به دنبال تغییرات ژنتیکی هستند که بیماریهایی مانند فشار خون بالا، دیابت و همچنین اختلالات روانپزشکی و عصبی مانند بیماری آلزایمر را توضیح میدهند، اغلب به تغییراتی نه چندان درون ژنها، بلکه بین آنها میرسیم.»
آن مناطق «بینابینی» همان تقویتکنندههایی هستند که تیم او اکنون مستقیماً در آستروسیتهای انسانی آزمایش کرده است – و نشان میدهد که کدام یک واقعاً ژنهای مهم مغز را کنترل میکنند.
«ما هنوز در مورد درمانها صحبت نمیکنیم. اما نمیتوانید آنها را توسعه دهید مگر اینکه ابتدا نمودار سیمکشی را درک کنید. این چیزی است که این به ما میدهد – دید عمیقتری به مدار کنترل ژن در آستروسیتها.»
از سوئیچهای ژنی تا هوش مصنوعی
آزمایش نزدیک به هزار تقویتکننده در آزمایشگاه کار دشواری بود. و این اولین بار است که غربالگری CRISPRi از تقویتکنندههایی در این مقیاس در سلولهای مغزی انجام میشود. اما با کارهای مقدماتی که اکنون انجام شده است، میتوان از دادهها برای آموزش ابزارهای کامپیوتری برای پیشبینی اینکه کدام تقویتکنندههای بالقوه سوئیچهای واقعی هستند، استفاده کرد و به طور بالقوه سالها در زمان آزمایش صرفهجویی کرد.
پروفسور ووینیگو میگوید: «این مجموعه دادهها میتواند به زیستشناسان محاسباتی کمک کند تا میزان کارایی مدلهای پیشبینی خود را در پیشبینی عملکرد تقویتکنندهها آزمایش کنند.»
او میافزاید: در واقع، تیم DeepMind گوگل در حال حاضر از این مجموعه دادهها برای ارزیابی مدل یادگیری عمیق اخیر خود به نام AlphaGenome استفاده میکند.
ابزارهای بالقوه برای ژندرمانی
از آنجا که تقویتکنندههای خاص فقط در انواع خاصی از سلولها فعال هستند، هدف قرار دادن آنها میتواند کنترل دقیق بیان ژن در آستروسیتها را بدون تأثیر بر نورونها یا سایر سلولهای مغزی امکانپذیر کند.
پروفسور ووینیگو میگوید: «اگرچه این روش هنوز به استفاده در کلینیک نزدیک نشده است – و کارهای زیادی قبل از اینکه این یافتهها به درمان منجر شوند، باقی مانده است – اما سابقه روشنی وجود دارد.»
«اولین داروی ویرایش ژن که برای یک بیماری خونی – کمخونی داسی شکل – تأیید شده است، تقویتکننده خاصی از نوع سلول را هدف قرار میدهد.»
مطلب مفید:
هوش مصنوعی میتواند تجویز دارو برای بیماریهای قلبی را متحول کند!
نورالینک (Neuralink): انقلاب در ارتباط مغز و کامپیوتر، از درمان بیماریها تا تعالی انسانی
دکتر گرین میافزاید که تحقیق در مورد تقویتکنندههای DNA یک جهت امیدوارکننده در پزشکی دقیق است.
او میگوید: «این چیزی است که میخواهیم عمیقتر به آن نگاه کنیم: فهمیدن اینکه از کدام تقویتکنندهها میتوانیم برای روشن یا خاموش کردن ژنها در یک نوع سلول مغزی واحد، و به روشی بسیار کنترلشده، استفاده کنیم.»
مرجع:
«غربالگری CRISPRi در آستروسیتهای انسانی کشتشده، تقویتکنندههای دیستال کنترلکننده ژنهای نامنظم در بیماری آلزایمر را آشکار میکند» نوشته نیکول اف. او. گرین، گوین جی. ساتون، خاویر پرز-بوریلو، جولی وانگ، ساموئل باگوت، هانا جی. دانون، کیران والش، آکیرا گوکول، سامانتا ای. مایلز، گوانگ یانگ، چارلز ای. هرینگ، یوهنگ لیانگ، گرانت پفوندشتاین، ولادیمیر سایتنیک، حمید علینژاد-رکنی، رایان لیستر، جوزف روزنبلو، یوهان ای. گاگنون-بارتش و ایرینا ووینگو، ۱۸ دسامبر ۲۰۲۵، نیچر نوروساینس.